 João Pessoa 28.13ºC
João Pessoa 28.13ºC Campina Grande 29.9ºC
Campina Grande 29.9ºC Patos 35.55ºC
Patos 35.55ºC IBOVESPA 158457.48
IBOVESPA 158457.48 Euro 6,53
Euro 6,53 Dólar 5,56
Dólar 5,56 Yuan 0,78
Yuan 0,78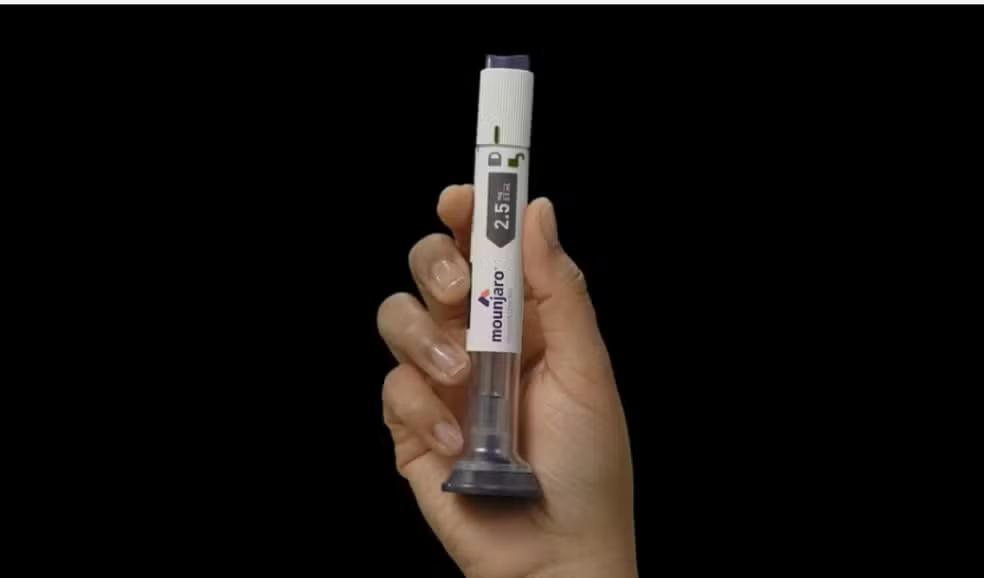
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quarta-feira (18), o registro de uma nova versão do Mounjaro, medicamento indicado para o tratamento do diabetes tipo 2.
A nova apresentação, chamada Mounjaro Multidose, permite que o paciente utilize uma mesma caneta aplicadora para mais de uma dose, diferentemente do modelo tradicional, de uso único.
A autorização está registrada na Resolução-RE nº 1.041, da Gerência-Geral de Medicamentos da Anvisa, e foi concedida à farmacêutica Eli Lilly do Brasil para o medicamento à base de tirzepatida.
A aprovação contempla seis diferentes concentrações do produto, todas em solução injetável de aplicação subcutânea: 4,17 mg/mL, 8,33 mg/mL, 12,5 mg/mL, 16,7 mg/mL, 20,8 mg/mL e 25 mg/mL.
A principal mudança com a aprovação da versão multidose está no formato do dispositivo. Enquanto o modelo tradicional de Mounjaro utiliza uma caneta para aplicação única, a nova apresentação permite que o paciente faça múltiplas aplicações com a mesma caneta. Esta alteração visa facilitar o tratamento, tornando o uso mais prático e conveniente para os pacientes com diabetes tipo 2.
A tirzepatida é um medicamento que age em hormônios relacionados ao controle da glicose e do apetite, contribuindo para o controle da doença e também para a redução de peso em pacientes.
A aprovação pela Anvisa autoriza a comercialização da nova versão no Brasil, mas a chegada do produto ao mercado dependerá de etapas posteriores, como a definição do preço e a estratégia de lançamento pela empresa.
Com informações do g1